早産児の消化管は未熟であるため、バリア機能の低下に伴って「リーキーガット」と呼ばれる臨床症状を引き起こすことがある。
リーキーガットでは、通常は腸管内腔に閉じ込められている細菌や細菌産生物が透水性が過剰になった上皮バリアを通過して末梢循環に移行することが可能なため、腸管上皮や腸管層の広範囲な侵襲、粘膜炎症、上皮細胞障害、腸管壊死、全身感染、ひいては多臓器不全、そして死に至る可能性がある。
壊死性腸炎 (NEC) は、早産児新生児の7~10%、新生児集中治療室 (NICU) 入室者全体の 1 ~5%で観察される細菌転座に関連した消化器疾患で、その破壊的な死亡率は50% にものぼる。新生児集中治療の進歩にも関わらず、NECは依然として罹患率と死亡率は低下しない。NECを含む合併症の発症を抑えるためには、リーキーガットの異常の早期発見と腸の損傷を抑えるための早期介入が非常に重要。
しかし、発達中の腸内細菌叢、栄養、腸管バリア機能の間の複雑な相互作用はほとんど解明されていない。
リンクのデータは、早産児113人の縦断的コホートの腸内細菌叢を特徴付けるために、16S rRNA遺伝子とメタゲノムの短時間および長時間シーケンシングを行った研究。
結果、Bifidobacterium breveの存在比が有意に高いことと、母親の母乳を多く含む食事が生後1週間の腸管バリア成熟と関連することがわかった。
上記の要因をゲノム分解メタゲノム解析により検討した結果、Bifidobacterium breve株はヒトの母乳オリゴ糖や宿主由来の糖タンパク質を同化する高度に特殊な遺伝的能力を持つことが明らかになった。
ビフィズス菌の特定株の存在は、異常な腸管透過性(IP)の早期発見につながる可能性があり、これらのビフィズス菌の補充は早産児のリーキーガットおよびその壊滅的な後遺症を予防するための新しい介入戦略に活用できる可能性がある。
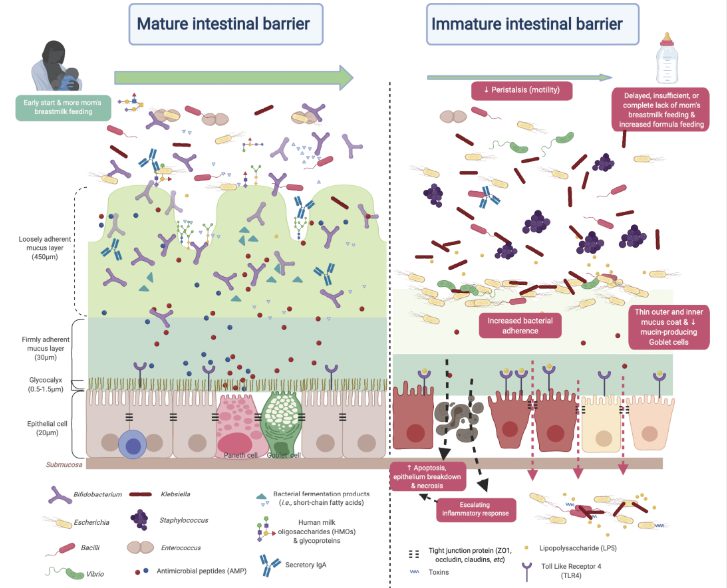
・早産の新生児は腸管バリア透過性が異常に高く、細菌移動を制限できないことが多い。
腸管透過性の持続的な上昇と摂食遅延、抗生物質への長期暴露、腸内細菌叢の発達の変化、およびクロストリジウム属細菌の漸増の欠如との間に正の相関があることを以前報告している。
クロストリジウム属細菌は生後2週目に多くなる。これは1週目に起こる広範なバリアーの成熟の後である。
・本研究では腸管透過性(IP)を有意に減少させるために必要な母乳の最小摂取量を決定し、特定のBifidobacterium種および菌株を、生後1週間の早産児の低IP発現に関連するバイオマーカーとして同定した。
・母乳の恩恵は栄養だけでなく腸管バリア機能の改善にも及ぶと考える。
IPの減少に関連する2要因(母乳栄養とビフィズス菌株)は、少なくとも部分的にビフィズス菌のヒト乳オリゴ糖代謝能力によって関連していると推定し、Bifidobacterium株の糖質代謝能力を評価し調査した結果、宿主由来の糖タンパク質と同様に多種多様なヒト乳オリゴ糖(HMO)分子を利用する遺伝子の相補性を見いだした。遺伝的特徴は、乳製品や成人の腸から分離された菌株と比較して、早産児の腸に関連するビフィドバクテリウム菌株に濃縮されていた。この結果は、ビフィズス菌優位の細菌叢の形成がHMO代謝を支える特定の遺伝子クラスターによって促進されることを示した先行研究の結果と一致する。
・ビフィズス菌の炭水化物消費による短鎖脂肪酸の産生、特に酢酸と酪酸は、抗炎症作用と相関し、上皮の防御機能を促進することが実証された。
・今回の結果は、腸管バリア機能は出生後に発達し、その過程は母乳基質およびそれらを消費するビフィズス菌の補充によって誘導されるという考え方を支持する。これらの要素は、NECや腸管透過性亢進に関連する生命を脅かす疾患を軽減する有望な治療標的である。
・B. breveは早産児および経産婦の腸内細菌叢において優勢なビフィズス菌種として知られ、母乳および膣内細菌叢でも観察された。ヒトでは、B. breveはこれらの環境にのみ存在し、成人の腸内環境にはほとんど存在しない。
・B. breveはHMOは、広範囲の食物および炭水化物を効率的に利用するための幅広い酵素能力を有し、乳児の腸内環境に最大限定着する。特に、LNnTの利用はB. breve株のみに限定されることが明らかになった。LNnTは、乳児の腸内にのみ存在するBifidobacteriumの特定の株によって発酵させることができる。
・B. breve株を早産児に投与した他の研究者による過去の臨床試験では、B. breve BBG株が未熟な腸管に効果的にコロニーを形成し、VLBW児の腹部異常徴候が有意に少なく、体重増加が大きいことを報告している。
・生きたバイオ治療薬の予防的補充における菌株の特性解析の重要性が浮き彫りになった。B. breve株が輸送・消費できるオリゴ糖の範囲を理解するためには、これらの重要な遺伝子のさらなる特性評価が必要であり、IPが急速に低下する早産児と健康な成熟児の両方から分離されたB. breve株のコレクションを確立することが必要。
・B. breveの特殊なHMOおよび糖タンパク質利用能力、特に硫酸化残基とシアル酸残基の分解能力はさらにB. breveの体力を向上させ、腸粘膜への付着とコロニー形成を促進する競争力を付与する。
・早産児への母乳はオリゴ糖結合シアル酸の豊富な供給源であり、シアル酸残基は満期産婦の母乳より20%、粉ミルクより25%多いことが報告されている。シアル酸やシアル化ラクト-N-テトラオースを利用できるのは、乳児腸管から分離したB. infantisとB. breveの菌株だけであることが報告されている。
・病原性を有する細菌がシアル酸を利用することから、B. breve株はシアル酸を病原体から速やかに隔離し、栄養を隔離して感染を抑えるという栄養免疫を提供し、健康な腸内環境の実現に貢献することが期待される。
・Bifidobacterium種によるHMO利用はもっぱら細胞内プロセスと思われ、他の腸内細菌種との中間体の交差供給が可能であるとは考えにくい。HMOを利用する際に「内部化してから分解する」というアプローチは、乳児の感染防御に重要なBifidobacteriumの特性。
・本研究は、早産児の腸管バリアを強化するために、HMOと共に特定のB. breve 株を生後早期に予防的に投与することの強い可能性を明らかにした。
以前の研究で、NECのようなリーキーガットに関連する疾患の発症前介入の「機会の窓」を出生後8日±2日と定義した。その重要な窓の期間中に母乳HMOを消費しうる有益なビフィズス菌種および菌株の増殖を促進する母乳栄養の役割を提案する。Bifidobacterium株が存在しない場合、母乳栄養の利点は劇的に減少すると予想される。
・母親の腸内細菌叢や膣内細菌叢、母乳からのビフィズス菌の垂直伝播に期待することは信頼性に欠け、多くの乳児を無防備のまま放置することになりかねない。ビフィズス菌を有効に利用する能力をもつバイオセラピューティクスを予防的に補充することで乳児の腸内でビフィズス菌に富む微生物叢が形成されるメカニズムについてさらなる理解を得ることが重要。