妊娠適齢期の女性における肥満の蔓延、罹患率の上昇は母体の健康上の問題だけでなく、子孫へ世代を超えた影響ももたらす。
実際に、糖尿病、心血管疾患、肥満、腎臓病の罹患率は、母親とその子孫の両方で増加している。
リンクのナラティブレビューは、母体の肥満が母体と胎児に及ぼす既知の影響、および母体と胎児の転帰に対する妊娠前または妊娠中の食事介入戦略の利点に焦点を当てている。
さらに、母体肥満げっ歯類モデルにおける疾患発症の生理学的経路の解明や、肥満が母体や発育中の胎児に与える影響を軽減する方法も検証している。
マウス研究とヒトでの研究データをまとめている貴重なレビュー。
一部専門用語が多く読みづらい面もあるかもしれないが、なるべく簡潔にまとめてみたい。
最近のいくつかのブログ(1)(2)とあわせて読んで頂ければと思う。
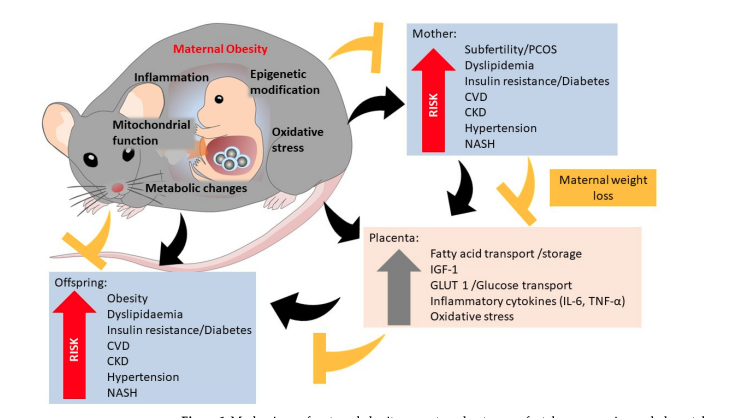
母親の体重減少が子孫のリスクを軽減するための潜在的な経路(黄色の矢印)。
*母親の肥満が母親の転帰に及ぼす影響
げっ歯類研究
マウスを用いた研究で、母親の肥満は母体の健康に悪影響を及ぼすという証拠が蓄積している。
母親の肥満は受胎能力の低下および自然流産の増加/胎児の再吸収と関連している。
また、母体のインスリン抵抗性および糖尿病リスクを増加させ、高血圧およびそれに伴う自律神経系の調節障害を引き起こす。
さらに、左心室質量の増加を伴う妊娠関連心肥大を誘発する。産後の持続的な母体肥満の影響には心肥大と心リモデリングが含まれ、妊娠と肥満の複合作用が心血管系の予後に有害であることが示唆されている。
遺伝的素因のあるラットでは、妊娠中および授乳期にHFDを与えると、母体の肥満と脂肪肝が引き起こされる。
母体マウスの飽和脂肪酸(SFA)大量摂取は、総コレステロール値およびLDL-コレステロール値に悪影響を及ぼし、その結果、酸化ストレスに対する感受性や動脈硬化の発症を促進することが示されている。さらに、脂質は特に生体内でシグナル伝達分子や転写活性化因子として作用する。
またSFAsは、脂質のホメオスタシス経路に関与する核内受容体に結合し、脂質滴の蓄積を誘導する。
肥満ネズミの脂肪組織と肝臓には、Tumour Necrosis Factor-αなどの炎症マーカーが確認されている。循環する炎症性サイトカインと遊離脂肪酸(FFA)は、さらにインスリン抵抗性を引き起こす可能性がある。
これらの知見は、肥満が誘発する代謝機能不全の経路が多面的でありながら交錯していることを示している。
肥満げっ歯類モデルにおいて、胎盤の異常が観察されている。
HFDを与えた肥満マウスの胎盤は胎盤の発達と血管形成に障害を示し、胎盤を介した栄養の伝達が減少することで、胎児の成長に変化をもたらすと考えられている。
また、肥満マウスの胎盤には慢性炎症が存在し、炎症性サイトカインの発現が増加している。
母親マウスの肥満は、子宮動脈およびらせん動脈のリモデリング低下と関連しており、胎盤不全を引き起こすという一貫した証拠が存在する。
DNAメチル化やヒストン修飾などのエピジェネティックなプロセスは、遺伝子配列に変更を加えることなくゲノム発現に遺伝的な変化を引き起こすため、胎児プログラミングの重要なメカニズムとして注目されている。
経胎盤におけるエピジェネティック・マシナリー遺伝子の発現の変化も証明され、遺伝子発現の変化は、経胎盤的なグルコース移行、胎児の成長、胎盤グリコーゲン、脂質の蓄積の増加に関連している。
ヒトでの研究
げっ歯類の研究と同様に、ヒトの妊娠における肥満関連の病態生理学的変化には、全身性炎症のアップレギュレーション、ホルモン異常、免疫学的調節異常が含まれる。
げっ歯類モデルで見られ胎児の過成長やマクロソミーは母体肥満の明確な結果であり、文献や臨床で十分に裏付けられています。
*母体の肥満はヒトの胎盤生理に影響を及ぼす
肥満女性の胎盤では炎症のアップレギュレーションが起こり、胎児では炎症マーカーの増加が検出される。
重度の肥満ではアディポカインの増加やサイトカインの放出が見られ、胎児の発育に影響を及ぼす。
母体のインスリンは胎盤のグルコース移行をGLUT4を介して刺激し、胎児へのグルコース移行を促進することから、高インスリン血症は胎児の過成長に重要な役割を担っていると考えられる。
母親の肥満は胎盤の代謝を変化させ、脂肪酸の酸化を増加させ、インスリン抵抗性とヒト胎児の血液中に見られる高い遊離脂肪酸濃度をさらに悪化させる。
*母親の肥満が胎児および子孫の転帰に及ぼす影響
げっ歯類の研究
げっ歯類の研究では、母親の肥満の結果として胎児の過成長が圧倒的に示されている。
出生後1日目という早期から周産期体重の増加が観察され、その後さらにHFDによって、体重増加、腹部脂肪率、循環コレステロール値がより速く上昇する。
母体肥満は胎児の腎臓のプライオトーシスとアポトーシスを増加させ、スーパーオキシドディスムターゼ2(SOD2)やカタラーゼなどの抗酸化物質の減少、酸化ストレスマーカーの増加などが示された。
また、母親の肥満は心臓発達に催奇形性を示し、大動脈弁の異常発達、内皮機能障害、血行動態の異常リスクが増加することが示された。
胎児の神経発達も母親の肥満によって変化し、妊娠17日目までに海馬に変化が見られることが分かった。
母体肥満モデルでは、胎児吸収の亢進も確認されている。
生後数日の成長不良や早期死亡は、肥満母マウスを持つ新生児と痩せた母マウスを持つ新生児でより一般的。
母体肥満が母体および新生児の周産期合併症に及ぼすメカニズムは知られているが、母体肥満が子孫の長期的健康に及ぼす影響は、特にヒトでの研究において確立されていない。
妊娠中の母親の肥満環境が、子孫の生涯にわたる代謝異常の決定因子であるという証拠がげっ歯類の研究で増えつつある。母親の肥満が子孫の代謝性疾患や肥満の発生を促進するという多くのエビデンスが蓄積され支持されている。
母親の肥満にさらされ、高カロリー食を与えられた子孫は、非アルコール性肝疾患のより高い傾向を示す。
さらに、肥満の母親の子孫は大動脈の脂肪酸組成に異常があることがわかった。
また、肥満マウスの16週齢の雄子孫の褐色脂肪組織代謝は、脂肪酸酸化、熱産生に関わる遺伝子のDNAメチル化の活性化が進み、褐色脂肪組織構造が損なわれていることが示されている。
マウスモデルでは、母親の肥満が世代を超えた心血管リスクに有害な影響を与えることが明確に示されている。左心室肥大と高血圧を伴う心臓のリモデリングが証明されている。
また、骨密度の低下と海綿体構造の調節障害も指摘されている。
母親の肥満が、成人後の肥満、糖尿病、心臓病などのメタボリックシンドロームの発症傾向の上昇と関連するメカニズムには、炎症、酸化ストレス、脂質代謝異常という重要な経路が関与することが知られている。
*母体肥満は子孫の不妊に影響を与える
肥満マウスのオス子孫では、精子のミトコンドリア機能の欠損やメタフェース異常の多発、活性酸素の増加など、精子の質と機能が損なわれていることが分かっている。
同様に、母親の肥満に暴露された子孫の卵子は肥満ではない母親の子孫の卵子と比較して、ミトコンドリア量と機能が低下していることが示されており、女性および男性の生殖能力に大きな影響を及ぼすことが示唆されている。
*母体肥満が子孫に及ぼすプログラミング効果は出生後の食事誘発性肥満によって増強される
過去の研究から、肥満の母親から生まれると、耐糖能の低下、インスリン抵抗性の増大、肝脂肪症、腎線維化など、肥満食の有害作用が著しく増強されることが明らかになっている
興味深いことに、肥満マウスの子どもは過食症になることも示されている。
げっ歯類モデルの母体肥満による発育プログラミングへの影響は子孫の性別によって異なる。
雄の子供は、雌の子供に比べ、体重、後腹膜脂肪量、肝臓量、血漿レプチン値、耐糖能異常が大きい。また、雌の子供に比べ、生後21日目の膵島数および分泌量が減少している。
*母親の肥満が子孫に及ぼす影響を裏付けるヒトでの研究
集団レベルのデータでは、肥満母親から生まれた成人した子孫は、主に心血管疾患によって引き起こされる早死リスクが高いことが示唆されている。
妊娠前の母親の体重が多いほど、小児期の脂肪率および脂肪分布が高いことが示されている。
妊娠中の体重増加は、母親の健康にとって重要なパラメータであり、マクロソミー、子癇前症、出産後の母親の肥満のリスク上昇と関連している。
さらに、妊娠中の体重増加は、乳児期における子孫の総脂肪率および体脂肪分布の独立した予測因子である。
母親の肥満環境は、高血圧、インスリン感受性の低下、有害な脂質プロファイルと関連している。
*妊娠中の食事調節と肥満母体および周産期予後への影響
げっ歯類試験
妊娠中肥満に対する介入戦略は、母体と胎児の両方の健康状態に影響を与える可能性がある。
しかし、げっ歯類モデルで妊娠中の体重調節のための介入戦略の効果を調べた研究はほとんどない。
ある研究では中鎖脂肪酸を強化し、多価不飽和脂肪を減らした脂肪酸組成変更食を利用し、非改良HFD給餌マウスと比較して母体の体重、脂肪細胞のサイズ、肝臓脂肪蓄積の減少、空腹時グルコース、インスリン、レプチン濃度が低下する傾向がみられた。
母体肥満のラットモデルで使用された魚油の補給は肥満とインスリン抵抗性を改善するようで、雄の子孫は成人期に脂肪率、肝炎、脂肪沈着が減少していた。雌の子孫はこの研究に含まれていない。
妊娠中に自発的な身体活動を増やすと、母親のインスリンおよびグルコース感受性が改善されるが、体重、妊娠期間、産児サイズ、新生児体重の減少には結びつかないことがわかった。
肥満母親の子孫は、痩せた母親を持つ子孫と比較して、体重が少なく、筋肉へのグルコースの取り込みが高く、血清インスリンレベルが低かった。
食事と運動の併用は、子孫のトリグリセリドレベル、グルコースレベル、インスリンレベル、酸化ストレスマーカーに有益な効果を示した。
ヒトでの研究
妊娠中の体重増加を抑制することで肥満関連の有害事象を減らすことを意図した妊婦を対象とした研究では、わずかな効果しか示されていない。
2152人の女性と2142人の新生児を対象とした妊娠中の監視下での生活習慣改善に関する大規模試験では、妊娠中の母親の転帰の改善も、新生児の罹患率の低下も見られなかった。
食事と運動の改善にプラスの影響を与えるための妊娠中の行動介入を利用した無作為化対照試験では、妊娠糖尿病発症率の低下、妊娠高年齢児の発症率の変化、子癇前症、その他の妊娠転帰を示すことはなかった。
残念ながら、妊娠中の体重増加を抑制する目的で、ヒトの妊娠期間中の食事変更を調査した研究では、出生時体重や新生児低血糖などの周産期転帰の改善は証明されていない。
これは、持続的な食事療法と行動修正の不足、妊娠による過食の影響、または体重関連の恒常性リセットの不足によるものである可能性がある。
根本的な原因が何であれ、妊娠が成立してからの体重調節は遅すぎるようだ。
*妊娠前の体重減少が母体、周産期および胎児の肥満関連アウトカムに与える影響
げっ歯類研究
母体肥満のげっ歯類モデルにおいて、妊娠前の体重調節が母体と胎児の健康に及ぼす影響を調査した研究はほとんどない。
研究には、食事療法、栄養補助食品、薬理学的薬剤、および外科手術による介入戦略が含まれる。
妊娠前の時期にネズミの食事をHFDからチャウに切り替えると、4週間の食事変更期間中にインスリン感受性、耐糖能、血清インスリンが徐々に改善されることが分かっている。さらに、コレステロール値も改善された。
6週間の継続的な減量により、卵母細胞のミトコンドリア構造の顕著な変化と反応性酸化ストレスレベルの改善により、生殖能力への恩恵が見られた。
また、妊娠前に母親の食事を変えることで、肥満の妊娠中マウスにおける脂肪肝を軽減できることが示された。
肥満マウスの子孫は、食事を切り替えた場合と比較して、脂肪細胞肥大が大きく、マクロファージの膨張や脂肪組織へのサイトカイン遺伝子発現が亢進していることが示された。
マウスの周産期予後に母親の運動が与える影響を調べた研究によると、耐糖能と末梢インスリン感受性の改善には、妊娠だけでなく、妊娠前および妊娠期間を通しての運動が最も効果的であることがわかった。これらの効果は母体の体重とは無関係で、トレーニングしても母体の体重に有意な影響を与えなかった。さらに、受胎率や子孫のサイズにも差はなかった。
*妊娠前の薬理学的介入は限られている
シタグリプチンを単独またはプロバイオティクス併用で妊娠前に使用することを検討した研究では、肥満母マウスの体重減少、インスリン感受性の改善、妊娠のアウトカムが認められたが、生殖機能の改善は見られなかった。
最近の研究では、妊娠前にリラグルチドを投与した肥満マウスにおいて、母体の体重減少、母体の耐糖能および脂質代謝の改善、出生率改善が示された。
母体肥満のHFD給餌げっ歯類モデルにおいて、急速かつ大幅な体重減少を促進するために、妊娠前の肥満手術の使用が検討されている。胃を80%切除する垂直スリーブ胃切除術を用いた研究では、カロリー摂取量、脂肪率、循環脂質、耐糖能が有意に減少し、生殖周期が正常化したことから、受胎可能性の予後が良くなったと推測される。しかし、子孫は、痩せた母親や偽手術を受けた肥満の母親の子孫と比較して、成長制限、耐糖能異常、脂肪率上昇を示した。
減量のための妊娠前の食事療法、運動療法、薬物療法は、母体と新生児の健康にとって有益であるという有望な兆候が示されているが、外科的介入による大幅な体重減少は、子孫に有害な結果をもたらす可能性がある。
ヒトでの研究
妊娠前の体重減少の利点については、ヒトでの研究はほとんど行われていない。
妊娠前期の低カロリー食は体重減少を誘発し、受胎率を向上させることができる。
食事の置き換えによるカロリー制限を調査したPre-babe Pilot Studyは、患者に受け入れられ、食事のみの場合と比較して、妊娠前の体重減少が顕著であったが、受胎可能性、母体および胎児の転帰に対する利点はまだ報告されていない。
12週間の減量プログラムを利用した前向き無作為化対照研究では、有意な体重減少、性 ホルモン結合グロブリンの増加、排卵が認められたが、平均LHまたはFSH濃度には変化はみられなかった。
多嚢胞性卵巣症候群の女性における6ヵ月間の体重減少を調べた同様の研究でも、妊娠率の改善が示された。
これらの研究を根拠に、不妊治療ガイドラインは妊娠前の体重減少を推奨している。
しかし、全体として、生活習慣のアドバイスの推奨の利点はまだ不明で、さらなる研究が必要。
妊娠前の肥満手術は、重度肥満の女性において妊娠前の体重減少を達成し,流産や先天性奇形の発生率を低下させて妊孕性を改善するための効果的なアプローチとなる可能性がある。しかし、減量手術は術後12カ月以内に妊娠した場合、ビタミン欠乏症、早産、妊娠年齢に対する小児転帰を引き起こす可能性がある。